Fiuto per i metalli
Fu così che tutto cominciò: avevo contattato un docente esperto in questo campo per avere dei consigli. Dopo aver curato in modo maniacale il testo dell’email, sbagliai inavvertitamente il titolo e scrissi: “Consigli per analisi fiutochelatine”. Considerando che il docente ha un esperienza decennale in “fitochelatine”, la reazione poteva essere di arrabbiatura o di ilarità; la sua intelligenza spostò l’ago della bilancia verso la seconda.
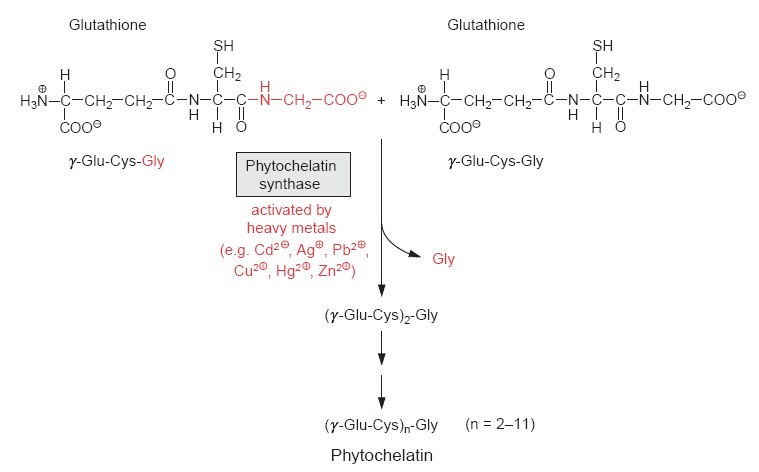
E fu così che mi appassionai di queste molecole molto strane. Derivano infatti dal glutatione, un tripeptide (cioè formato da tre amminoacidi, nell’ordine: glutammato, cisteina e glicina). Il glutatione è già parecchio importante nelle piante, in quanto è un forte antiossidante (un po’ come la vitamina C) e quindi protegge le piante da vari tipi di disturbi. Più molecole di glutatione (da 2 fino a 11) si legano e formano le fitochelatine, che sono una specie di catene di molecole di glutatione unite l’una con l’altra. La sintesi delle fitochelatine, in vivo, richiede la presenza di glutatione ed è catalizzata dall’enzima g-glutammil-cisteina dipeptidil transpeptidasi (per gli amici, fitochelatina sintetasi), i cui geni sono stati recentemente identificati ed isolati nella pianta-modello Arabidopsis thaliana, nel frumento, nel lievito e sorprendentemente anche nel nematode (questo è un animale!) Caenorhabditis elegans.
 Figura 1. In alto: sintesi delle fitochelatine. In basso: ione cadmio “chelato” dagli atomi di zolfo delle cisteine (fonte: Heldt, 2005).
Figura 1. In alto: sintesi delle fitochelatine. In basso: ione cadmio “chelato” dagli atomi di zolfo delle cisteine (fonte: Heldt, 2005).
Come spesso accade in Natura – ed estenderei questa legge anche ai comportamenti umani – l’unione delle singole parti è maggiore della semplice somma delle singole parti. Alla fine, quello che ne risulta ha proprietà completamente diverse da ciò che si aveva all’inizio (“teoria delle proprietà emergenti”, la chiamano). Vale in questo caso anche il “principio di massima economia”: il tutto parte da tre amminoacidi utilizzati normalmente per formare proteine, poi c’è la sintesi del glutatione, e infine delle fitochelatine. Ad ogni livello è associata una funzione diversa. Inoltre, la sintesi di fitochelatine è indotta dalla presenza di metalli nel suolo a partire dal glutatione, i cui livelli quindi diminuiscono.
Mentre il glutatione è un antiossidante, le fitochelatine hanno un compito completamente diverso: proteggono le piante dai metalli per loro tossici, come cadmio, argento, piombo, rame, mercurio e zinco. Gli ioni di questi metalli presentano quasi tutti delle cariche più o meno positive e, una volta entrati dal suolo nelle cellule della radice, vengono catturati (“chelati”, da cui il nome “fito-chelatina”) dalle cariche negative delle fitochelatine (presenti sugli atomi di zolfo dell’amminoacido cisteina). A questo punto, i metalli pesanti sono portati, a spese di energia, in un contenitore nella cellula (vacuolo) e là stipati come inoffensivi sotto forma di solfuri o acidi organici. Le fitochelatine tornano allora indietro bel citoplasma per catturare di nuovo un altro metallo; e il ciclo ricomincia. In questo modo, le piante rendono i metalli inoffensivi perché li conservano in una specie “sgabuzzino” cellulare.
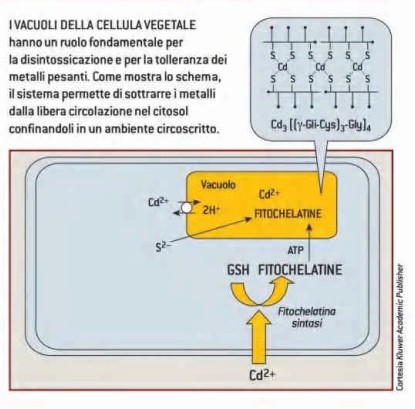 Figura 2. Meccanismo di azione delle fitochelatine (fonte: Sanità di Toppi, 2002).
Figura 2. Meccanismo di azione delle fitochelatine (fonte: Sanità di Toppi, 2002).
Le fitochelatine sono peptidi molto speciali. Prima di tutto, a differenza di molti peptidi, non sono sintetizzate sui ribosomi, ma nel citoplasma a partire da glutatione. Il gene che le esprime (fitochelatina sintasi) è quasi sempre attivo, sia in presenza che in assenza di metalli pesanti, sia in specie sensibili che in specie tolleranti. Ciò significa che la regolazione avviene probabilmente anche a livello post-trascrizionale e che non sono solo le fitochelatine a determinare la suscettibilità/tolleranza di una pianta ai metalli pesanti. Probabilmente c’entrano anche altri meccanismi, quali il trasporto e l’immagazzinamento nei vacuoli, e la sintesi di altri composti contenenti zolfo (es. metallotionine), la secrezione di essudati radicali, produzione di legno, sintesi di altri composti, ecc. ecc.
I metalli con cui le fitochelatine hanno più affinità sono argento, arsenico, cadmio, rame, mercurio, piombo e zinco. Le fitochelatine sembrano essere essenziali per l’omeostasi e il metabolismo per questi ioni, in particolare per il cadmio. A titolo di esempio, mentre metalli come rame e zinco, sebbene a basse concentrazioni, sono utili al metabolismo cellulare e risultano tossici solo ad alte concentrazioni, il cadmio è inutile per le piante ed è normalmente presente in bassissime concentrazioni nei suoli (0.3 µM), e quindi è molto tossico. I suoli inquinati da cadmio sono per il 99% opera dell’uomo (fanno eccezione i suoli serpentinosi, ad esempio); e l’inquinamento, si sa, è cosa recente. Le fitochelatine, d’altro canto, sono molto antiche. L’enigma si infittisce perché le fitochelatine sono attivate soprattutto dal cadmio in concentrazioni superiori a 1.0 µM, cosa che non si verifica praticamente mai se non in suoli inquinati dall’uomo. Sembra quindi che le fitochelatine diano tutto il loro vantaggio in suoli inquinati e non in condizioni naturali!
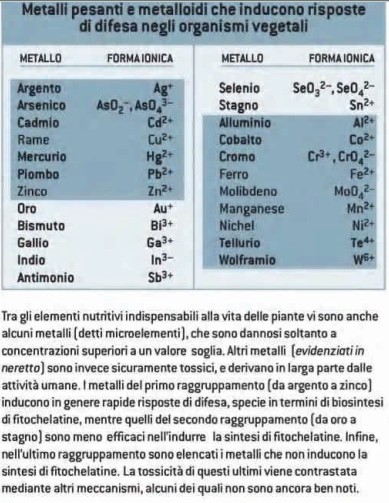 Figura 3. Metalli e loro affinità per le fitochelatine (fonte: Sanità di Toppi, 2002).
Figura 3. Metalli e loro affinità per le fitochelatine (fonte: Sanità di Toppi, 2002).
Sono state fatte varie ipotesi a riguardo. Ne azzardo due:
1) Le fitochelatine e l’apparato per sintetizzarle sono molto molto antiche, probabilmente già presenti in un ancestore comune a piante, funghi e animali. In condizioni primordiali, le acque in cui questi organismi vivevano erano ricche di metalli pesanti, probabilmente provenienti da materiale magmatico, ed essi avevano la necessità di detossificare tutti quei metalli. Già alcuni composti solforati assolvevano questo compito, ma la comparsa delle fitochelatine fu un ulteriore vantaggio evolutivo.
2) Le fitochelatine sono un esempio di “esattamento” (“exaptation”): nate per una funzione, alla fine ne hanno acquisita un’altra completamente diversa. La disattivazione di composti tossici (erbicidi, pesticidi, metalli pesanti) per mezzo di composti solforati è sempre presente, anche in maniera latente, nelle cellule. L’alta affinità per il cadmio potrebbe essere allora un puro caso, e il mantenimento delle fitochelatine – a che servirebbero, infatti, senza il cadmio? – dipende dal fatto che comunque hanno affinità per molti metalli. Si è ipotizzato anche che fungano da veicoli di ioni metallici per far funzionare alcuni enzimi, o ancora che permettano alle piante di accumulare metalli per essere poco appetibili agli insetti. Inoltre, la loro via biosintetica è, almeno all’inizio, comune a cisteina e glutatione, composti entrambi indispensabili sia a cellule vegetali che animali (se chiedete un passaggio per un posto, all’autista non costa niente lasciarvi prima se fa la vostra stessa strada).
Lo studio delle fitochelatine ha anche fini pratici. Si possono infatti usare le piante per bonificare siti inquinati da metalli pesanti (fitorisanamento). Questa è un’altra storia ma, se siete curiosi, guardate il filmato in basso. Dubito che le fitochelatine abbiano fiuto anche per l’uranio, ma forse il video rende lo stesso l’idea.
Grazie a loro, ho scritto:
Anonimo. Tesi di laurea disponibile su http://biochimica.unipr.it/home/tesi/att/37bc.testo.doc
Christopher S. Cobbett (2000) Phytochelatins and Their Roles in Heavy Metal Detoxification. Plant Physiology, July 2000, Vol. 123, pp. 825–832
Hans Lambers, F. Stuart Chapin III, Thijs L. Pons (2008) Plant Physiological Ecology – Second Edition. Springer Inc.
Hans-Walter Heldt (2005) Plant biochemistry – Third Edition. Elsevier Inc.
Luigi Sanità di Toppi (2002) Le difese delle piante dai metalli pesanti. Le Scienze 404: 88-92.
Neil Willey (2007) Phytoremediation. Humana Press Inc.