Questo che pubblico oggi è il post che ho scritto per il Carnevale della Biodiversità 2011. Spero vi piaccia. Il tema di quest’anno era “Biodiversità e adattamenti; la lotta costante per il cibo e per lo spazio“. Grazie a Lisa per l’invito e a Marco per la pazienza!
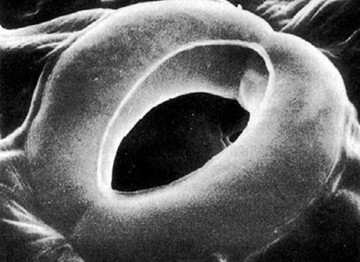
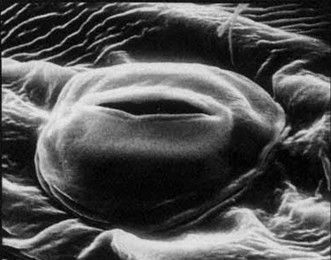
Sono stato a lungo indeciso sull’argomento di questo post (grazie Lisa!). Ho vagato con la mente dalle “exaptations” di gouldiana concezione applicate all’assorbimento di metalli pesanti al “barcoding” delle specie vegetali, ma mi sembravano idee astratte e artificiali nate da campus del nuovo mondo e da laboratori metropolitani, e invece a me serviva un’idea “terra terra”, nel senso etimologico e buono del termine, e non filosofica o “troppo molecolare”. Alla fine, l’ “illuminazione” è arrivata, come sempre, dall’esperienza vissuta. Ho ripescato le foto delle mie camminate e l’idea, latente, era là (Foto 1-3). La lotta costante per il cibo e lo spazio era sotto i miei occhi ma, temporaneamente distratto dal panino con la frittata nello zaino, non me n’ero accorto. Qualche mese fa, a Serra di Crispo sul Massiccio del Pollino, alzando lo sguardo, avevo detto al mio amico di viaggio che la scena mi sembrava quella di un assedio di faggi alle ultime roccaforti di pino. In realtà, non era un pino qualunque, ma il simbolo del Parco Nazionale del Pollino: il pino loricato. Gli alberi ergevano come fantasmi pallidi e corazzati, corazzati come coccodrilli (loricati entrambi!), dai lenti movimenti (anche le foreste si muovono!) come le tartarughe, testimoni di un passato remoto. Ma basta con la pseudo-poesia e torniamo alla xerofila scienza.
Il pino loricato (Pinus leucodermis Antoine) è un albero raro nonché uno dei più antichi dal punto di vista filogenetico. E’ presente soprattutto all’interno del Parco del Pollino, dov’è presente dalla fascia montana a quella alto-montana ma scende nel settore sud-ovest anche a quote più basse fino a raggiungere i 535 s.l.m. Nel 1863, il botanico tedesco Hermann Christ identificò un nuovo pino da campioni provenienti da ristrette zone montuose della Serbia, del Montenegro e della Grecia settentrionale, e lo chiamò “Pinus heldreichii Christ.”, in onore del suo scopritore, nonché grande botanico, Thoedor Von Heldreich. Nello stesso periodo, un albero simile venne descritto dal botanico Antoine che, evidenziando il colore chiaro della corteccia, gli assegnò il nome di Pinus leucodermis. Nel 1906, il botanico napoletano Biagio Longo studiò i campioni da lui raccolti sul Pollino attribuendoli alla specie “Pinus Leucodermis Antoine”, e coniò il nome di “pino loricato”. Notò infatti che la corteccia della pianta adulta si fessurava in caratteristiche placche poligonali che ricordavano la corazza dei soldati romani, chiamata appunto “lorica” (“thõreka”, “torace”, in greco antico, e “lorica” in latino) (Foto 4). Insomma, un pino la cui corazza è indispensabile per riuscire a resistere alle intemperie che flagellano i crinali del Pollino.

Foto 1. Pini loricati “sotto assedio” (Serra di Crispo, Parco Nazionale del Pollino; foto mie).

Foto 2. Pini loricati a Serra di Crispo (foto M. Campochiaro).

Foto 3. “Sentinelle” isolate di pino loricato “scrutano” l’esercito di faggi sottostante (Serra di Crispo; foto mia e A. Castelmezzano).

Foto 4. Lorica e pigne di pini loricati a Pietra Castello (a sinistra in alto; foto A. Castelmezzano) e a Serra di Crispo (le restanti, foto mie).
Ma, alla fine, si tratta di una specie con due varietà o di due specie distinte? Sono due ma la loro origine è la stessa. Due, proprio in base alla classica e scolastica enunciazione di specie di Dobzhansky e Mayr: oramai non si incrociano più reciprocamente. L’areale della specie ancestrale sembrerebbe (il condizionale è d’obbligo perché fossili e prove certe non ce ne sono) sia stato quello balcanico. I semi alati e leggeri, lunghi fino a circa 6-7 mm, sarebbero giunti nell’Italia meridionale nel Pliocene (da 5,3 a 2,6 milioni di anni fa, quando era un vero e proprio pantano), probabilmente per saltazione, cioè un po’ svolazzando, un po’ impantanandosi e germinando nei vari isolotti che incontravano, fino ad arrivare agli adolescenti Appennini (Foto 5). In seguito si sarebbe verificata una speciazione allopatrica: secessione e ciascuna specie per conto suo. Anche visivamente, si nota subito che in Pinus leucodermis la corteccia dei rami giovani si mantiene per molti anni liscia, lucente, di color cenere chiaro con areole squamiformi che ricordano la pelle di un rettile, e gli strobili (che a me è sempre piaciuto chiamare pigne) hanno la parte esterna della squama (apofisi) di forma piramidale; invece in Pinus heldreichii la corteccia dei rami giovani si scurisce precocemente e gli strobili presentano un’apofisi appiattita.

Foto 5. L’Italia Nel Pliocene (fonte:http://www.naturamediterraneo.com/forum/topic.asp?TOPIC_ID=47403).
Il Pollino è un massiccio molto particolare e ricco di biodiversità perché tra le sue montagne convivono allegramente elementi di tipo artico-alpino, elementi medio-europei, mediterranei, balcanici oltre ad un consistente numero di endemismi e di specie sopravvissute alla flora del Terziario (da 40 a 2,5 milioni di anni fa, di cui il Pliocene è l’epoca finale). Il pino loricato è stato ed è ancora definito “un paleo-endemismo terziario con areale anfi-adriatico”, “un elemento balcanico ad areale disgiunto”, “un relitto delle foreste a conifere mediterranee della penisola Balcanica e dell’Appennino meridionale”. Ma continuiamo pure a denigrarlo, e chiamiamolo anche “fossile vivente”, “relitto delle ere glaciali”, “scherzo della natura”, “stranezza del Creato”, ecc. ecc., tanto queste definizioni-clichès sono difficilmente dimostrabili e spesso scientificamente inesatte, e quindi non lo tangono più di tanto.
In Italia, la specie, ampiamente diffusa sui rilievi carbonatici sub-montani e montani dell’Appennino meridionale nei periodi secchi del Pliocene, ha subito un rapido declino nelle fasi glaciali del Quaternario che si manifestarono nell’Appennino meridionale, con modificazioni climatiche in senso fresco e umido (una mazzata per le conifere, amanti dei climi freddi ma secchi). Oggi, a fare buona compagnia al pino loricato ci sono altre specie che prosperavano nel Terziario, come l’agrifoglio, l’alloro e il tasso, guarda caso tutte specie arboree ricchissime di significati simbolici fino al Medioevo, come se la loro antica origine li abbia resi venerabili (imprinting degli alberi pliocenici sugli ominidi? Questa la suggeriamo a Roberto Giacobbo). Queste specie hanno trovato rifugio nella vegetazione post-glaciale e si rinvengono prevalentemente nella fascia di transizione tra i boschi di querce mesofile (vegetazione sannitica) e la faggeta (vegetazione subatlantica). Attualmente, l’areale di Pinus leucodermis gravita nel settore di influenza tirrenica (più freddo del suo compagno adriatico, con cui sul Pollino va a braccetto) dove prevalgono substrati carbonatici (calcari e dolomie del Mesozoico) ad elevata xericità, associati ad una morfologia rupestre. La specie è quindi esigente: preferisce il freddo, ma secco, e i substrati calcarei.
Ora rivolgo l’attenzione ai suoi avversari per il cibo e lo spazio, se no, tra incidentali e divagazioni varie, esco fuori tema e vengo bacchettato. Dopo l’ultima glaciazione del Quaternario (conclusasi 13500 anni fa), quando il ghiaccio copriva ancora molte zone montane, le foreste appenniniche erano limitate alle zone centro-meridionali. La facevano da padrone due specie oggi a distribuzione più marginale: guarda caso, proprio il pino loricato e il pino silano (Pinus nigra subsp. laricio; da calabrese, propendo campanilisticamente verso il secondo), con presenza sporadica di abete rosso (Picea abies L.). Successivamente, a causa del progressivo riscaldamento, comparvero i primi consorzi misti ad abete bianco (Abies alba Mill.) e faggio (Fagus sylvatica L.), l’abete rosso (quasi) scomparve gradualmente dagli Appennini, e le pinete si spostarono sempre più verso sud. Ma il caldo avanzava, e tra 10300 e 8800 anni fa (inizio dell’Olocene) era l’abete bianco che spopolava sugli Appennini, diventando così predominante. I pini si ritirarono verso la sommità dei rilievi. Nel frattempo, il subdolo faggio, di provenienza atlantica e desideroso di climi oceanici, all’arrivo delle glaciazioni si ritirò sulle montagne del Sud, ma era pronto a ripartire e ad espandersi con l’arrivo della bella stagione postglaciale, a danno delle querce e dei pini. E infatti, con l’instaurarsi di climi sempre più caldi e umidi (tra 7500 e 4500 anni fa), la diffusione del faggio sugli Appennini meridionali subì una forte accelerazione, raggiungendo l’optimum climatico circa 2.500 anni fa.


Foto 6. Pendii xerotermici a Serra di Crispo (foto in alto Mirella Campochiaro, le restanti mie).
Oggi, la fascia montana del Parco del Pollino, è anche detta subatlantica in quanto, al di sopra dei 1000 m, c’è un clima che si avvicina a quello diffuso nel Nord-Ovest dell’Europa, in prossimità dell’Oceano Atlantico, dove infatti le pianure, poste a livello del mare, ospitano estese faggete, analogamente alle montagne appenniniche. Tale clima è caratterizzato da discreta piovosità estiva e frequenza di nebbie, unitamente a temperature non eccessivamente alte. Qui, i boschi a faggio rappresentano le formazioni predominanti fra i 1100 e i 1800-1900 m; sul versante tirrenico, più fresco, non sono rare formazioni anche miste al di sotto di tale fascia, fino agli 800 m, e in ambienti di forra, anche a 500 m. Sul versante nord del Parco (Monte Sparviere, Piano di Iannace), le faggete vedono anche una cospicua partecipazione di abete bianco, il quale, presso il Bosco Vaccarizzo, scende a quote eccezionalmente basse. L’abete bianco, nel Parco, non si spinge quasi mai sui crinali più alti, eccetto che su Serra di Crispo, e quindi difficilmente compete con il pino loricato, anche perché predilige substrati argillosi. Le faggete dei massicci carbonatici del Pollino, invece, ampie e rigogliose, sfiorano i 2000 m e sono a diretto contatto con il loricato.
Questo, al contrario del faggio, non forma mai dei popolamenti chiusi, ma piuttosto delle pinete aperte in stazioni sfavorevoli al faggio, come ad esempio sui pendii xerotermici rivestiti da praterie (Monte La Caccia, Montea, Serra di Crispo, ecc.) (Foto 6-7). Frequenti sono gli esemplari isolati, anche di notevoli dimensioni, su costoni rocciosi, cenge rupestri (Pollinello, Colle Dragone). Grazie alle notevoli capacità di adattamento all’aridità del suolo, il loricato riesce a vivere al di sopra del limite del faggio; infatti, sulle rupi del versante meridionale della Catena del Pollino, diversi sono gli alberi vetusti attorno ai 2100 m. La bellezza unica dei boschi del Pollino è proprio questa: è l’unico esempio appenninico di una certa consistenza in cui una formazione di conifere arboree (il loricato) si colloca al di sopra della faggeta. C’è poco fare: le due specie sono in guerra per lo spazio ma anche per il “cibo”: entrambi preferiscono i substrati calcarei e scappano a radici levate davanti ai terreni argillosi. Dopo quella dai Balcani, quindi, la seconda migrazione, forzata, del loricato è stata quella in senso “verticale”, a causa della pressione del faggio, più forte e invadente.

Foto 7. Anfiteatri naturali di pino loricato a Serra di Crispo (foto mie).
Da biologo rompiscatole, mi chiedo però se tutte queste migrazioni del loricato siano dovute solo a cambiamenti climatici/microclimatici o anche ad altro. Cerco in bibliografia e trovo che il loricato si riproduce in modo estremamente faticoso e lento: la germinazione del seme richiede di due anni, a fronte dei 10-15 giorni occorrenti ai semi delle altre conifere, e l’accrescimento risulta 6-7 volte più lento che in altre specie di conifere (caso unico)! D’altro canto, è un albero molto longevo, potendo arrivare anche a 900-1000 anni (esemplari sul versante calabrese del Pollino) e quindi ha parecchio tempo per lasciare discendenti. Il suo legno è estremamente resinoso e ricchissimo di sostanze fenoliche ad effetto antimicrobico, antiparassitario e allelopatico. Non a caso, questa caratteristica porta a processi di marcescenza molto lenti dopo la morte della pianta, con l’ulteriore e suggestivo effetto di piante non più in vita ma che non crollano al suolo e restano erette per anni, trasformandosi in veri e propri monumenti arborei, “generatori” di nicchie ecologiche per insetti, nematodi e uccelli (Foto 8). Anche da vivo, però, la corteccia del loricato ospita una fauna varia e preziosa, come Buprestis splendens, un buprestide, unico in Italia, legato ai climi freschi mediterranei, ma anche altri coleotteri (buprestidi, curculionidi, scotilidi e ostomidi), o farfalle, tra cui il satiride Erebia gorge; e ancora, vertebrati come lo scoiattolo meridionale melanico (snello ed elegantissimo, con la sua pettorina bianca), la lucertola muraiola che si crogiola al sole sulle radici sporgenti, e uccelli come la cinciallegra, la cincia mora, il codirosso, il merlo del collare, il picchio nero e il picchio muratore (Foto 9).

Foto 8. Anche da morto, il pino loricato ha una funzione importantissima per il bosco, sia dal punto di vista ecologico che paesaggistico (foto mie).

Foto 9. Buprestis splendes (http://www.biolib.cz/en/image/id67420/), scoiattolo melanico (Sciurus vulgaris var. meridionalis) (fonte: http://www.provediemozioni.it/index.php?pag=Scoiattoli) e maschio di crociere comune (Loxia curvirostra L.; foto mia).
Quale specie delle due “vincerà” la competizione per lo spazio? Il tutto dipende dalla scala di tempo considerata. Nell’immediato sembra che il loricato abbia la meglio sul faggio in quanto a difese dovute al suo metabolismo secondario (es. sostanze allelochimiche o repellenti per gli erbivori, escrezione di essudati radicali acidi che solubilizzino nutrienti difficilmente disponibili, ecc.). La sua resina, acida e ricca di composti fenolici semplici e complessi, è un forte antimicrobico che lo preserva da marciumi e batteriosi. Un’altra barriera efficace contro i patogeni e contro gli agenti atmosferici (fulmini compresi) è costituita dalla sua corteccia fortemente lignificata e suberificata. La struttura aghiforme e la disposizione compatta delle foglie ed il colore chiaro della corteccia, poi, permettono al pino loricato di riflettere la maggior parte della forte luce incidente (a 2000 m non si scherza), conservando solo quella che serve per la fotosintesi ed evitando così fenomeni di foto-inibizione. E’ stato altresì trovato che la traspirazione fogliare e la conduttanza stomatica in questa specie sono finemente regolate, per evitare di perdere troppa acqua a causa della bassa umidità dell’aria delle zone in cui cresce. Infine, le radici, robuste e plastiche allo stesso tempo, permettono alle piante di crescere e ancorarsi su rocce calcaree inaccessibili ad altre specie arboree, spesso su pendii fortemente scoscesi e su crinali che circondano precipizi. In un’ottica più ampia però, il faggio mostra una maggiore plasticità fenotipica (efficienza fotosintetica, struttura dei vasi xilematici, tasso di crescita) che gli permette un maggiore successo competitivo nelle condizioni attuali. E la mazzata finale al pino (e all’abete bianco) è costituita dal fatto che si riproduce non solo da seme ma per polloni (Foto 10), e che il suo legno non è poi così pregiato (gli abeti bianchi appenninici, ma anche i pini, hanno conosciuto molto bene le scuri umane! Recenti studi dendrometrici e dendrocronologici hanno dimostrato che anche l’uomo ed il pascolo hanno fatto la loro parte, insediando ancora di più la sopravvivenza del pino loricato (con qualche eccezione, come l’enorme incendio del 1948 sul monte della sulla Spina che lo ha favorito).

Foto 10. Faggi sui Piani di Acquafredda, Parco del Pollino. Si notano i numerosi polloni, diventati quasi tutti fusti principali (foto mia).
Il rettile vegetale ha perso? 4, 5… E’ quasi ko, messo al tappeto nell’angolino calcareo e secco del ring. 6, 7… E’ alle corde, ovunque attorniato da faggi. 8, 9… ma ecco che si rialza e pensa: “Quando il gioco si fa duro, i duri cominciano a giocare” (Belushi J. et al., 1978).
Le condizioni climatiche e geopolitiche sono mutevoli, così come le specie che più o meno le seguono, e la situazione sta cambiando. Il clima del meridione, sta diventando sempre più caldo, ma anche più secco, e andando avanti così il faggio si ritirerà ed il loricato scenderà di nuovo in basso. Sembra quindi che ci sia un lento ma inesorabile ritorno al clima pliocenico e che il faggio avrà la peggio perché richiede un regime pluviometrico con precipitazioni uniformi durante tutto il periodo vegetativo. Osservazioni recenti testimoniano che, soprattutto al Sud, il faggio si sta ritirando, anche se lentamente. Un’altra prova a favore di questa ipotesi è che in Calabria (Pollino meridionale, Verbicaro, Orsomarso), dove il clima è più secco a causa della barriere costituita dal Pollino stesso, il pino loricato non si limita a permanere nella fascia subalpina, ma scende ampiamente nella zona del faggio, tanto da entrare quasi a contatto con la lecceta. E il faggio sta cedendo anche su altri fronti. Ad esempio, sul Monte Sparviere, nulla catena orientale del Massiccio del Pollino, una volta c’era la faggeta, poi soppiantata dal bosco misto a prevalenza di ontani ed aceri. Non per altro qui sono rimasti anche gli abeti bianchi, xerofili, favoriti dalla presenza di rocce marnoso-arenacee, non adatte al loricato.
Il pino loricato, in declino fino ad una ventina di anni fa, appare ora in recupero grazie alla forte riduzione del pascolo e alla maggiore protezione (anche se a volte rimane sulla carta) e, specialmente nei suoi habitat di elezione, non è infrequente un attivo rinnovamento. Continuando così, potrebbe di nuovo espandere il suo areale, ripartendo proprio dalle montagne dell’Appennino meridionale. Anche per questo il pino loricato mi ricorda i coccodrilli, che restano nascosti sott’acqua e appena adocchiano la preda hanno dei rapidi scatti. Chi vivrà, magari 900 anni come i grandi Patriarchi del Pollino, vedrà.

Foto 11. A sinistra (foto A. Castelmezzano), pini loricati immersi nella faggeta (Timpa del ladro, Parco del Pollino). A destra (foto mia), splendido esemplare di pino loricato a Serra di Crispo.
Grazie a loro, ho scritto:
- Avolio S (1992) L’acquisizione forestale del pino loricato (Pinus leucoderma Antoine). Estratto da L’Italia Forestale e Montana Anno XLVII – Fase. n. 4: 211-227, Luglio-Agosto 1992. Firenze, Tipografia Coppini.
- Bernardo L (2010). Pino loricato: non chiamiamolo “fossile vivente”! Apollinea, nov-dic 2010: 16-17.
- Bernardo L (2001). Fiori e Piante del Parco del Pollino, 3a edizione. Edizioni Prometeo.
- Castelmezzano, A. (2011) Escursioni, chat e chiacchierate con il grande esperto A. Castelmezzano (anche se non lui non lo sa!)
- I boschi montani di conifere (2007) Quaderni Habitat. Ministero dell’Ambiente e della Tutela del Territorio e del Mare – Museo Friulano di Storia Naturale.
- Il pino loricato. Reperibile su http://www.terranostrabasilicata.it/default.aspx?pagina=pino
- Lambers H, Stuart Chapin III F, Pons TL (2008) Plant Physiological Ecology – Second Edition. Springer-Verlag.
- Lange W, Janezic TS, Spanoudaki M. (1994) Cembratrienols and other components of white bark pine (Pinus heldreichii) oleoresin. Phytochemistry 35: 1277-1279.
- Le faggete appenniniche (2006) Quaderni Habitat. Ministero dell’Ambiente e della Tutela del Territorio e del Mare – Museo Friulano di Storia Naturale.
- Omasa K, Nouchi I, De Kok LJ (2005) Plant Responses to Air Pollution and Global Change. Springer-Verlag.
- Schulze E-D, Beck E, Müller-Hohenstein K (2002) Plant Ecology. Springer-Verlag.
- Tassi F (1998) Studi sulla fauna del Pollino. Studi per la conservazione della natura, vol. 26; Ente Autonomo Parco Nazionale D’Abruzzo. Ed. Almadue srl, Roma.
- Thompson JD (2005) Plant Evolution in the Mediterranean. Oxford University Press.
- TodaroL, Andreu L, D’Alessandro CM, Gutiérrez E, Cherubini P, Saracino A (2007) Response of Pinus leucodermis to climate and anthropogenic activity in the National Park of Pollino (Basilicata, Southern Italy). Biological Conservation 137: 507-519.
- Willis KJ, McElwain JC (2002) The Evolution of Plants. Oxford University Press.
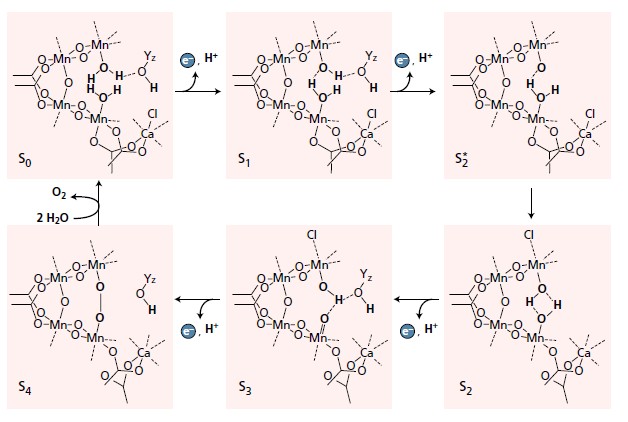
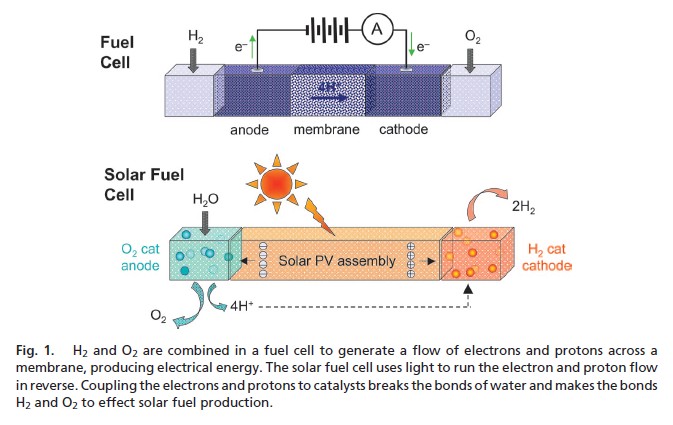
 La separazione di protoni (H+), elettroni e ossigeno in una foglia artificiale (fonte: Gray, 2009)
La separazione di protoni (H+), elettroni e ossigeno in una foglia artificiale (fonte: Gray, 2009)