Quanto funziona la fotosintesi?
[Questo articolo è stato ispirato, rielaborato e in parte riprodotto da “La Fisica della Vita”, Jim Al-Khalili e Johnjoe McFadden, ed. Bollati Boringhieri].
In un articolo di parecchi mesi fa pubblicato su questo blog avevo scritto che un organello cellulare chiamato cloroplasto è responsabile della fotosintesi nelle cellule vegetali. I cloroplasti sono molto particolari perché derivano da batteri indipendenti che probabilmente, miliardi di anni fa, sono entrati in simbiosi obbligata con antiche cellule eterotrofe che non facevano fotosintesi. Quest’ultima è un processo molto complesso, che coinvolge decine di enzimi, proteine che, per le loro reazioni chimiche specifiche e rapide, possono essere definiti le macchine della vita. Basti pensare che in un solo secondo, le piante e i microbi fotosintetici raccolgono la luce solare e creano circa 16.000 tonnellate di nuova materia organica, quasi tutta la biomassa del pianeta.
Ora, la gran parte dei biologi pensa che le leggi classiche, spiegabili con le leggi newtoniane, siano sufficienti a spiegare la fotosintesi, dal momento che le biomolecole e gli enzimi coinvolti si comportano proprio come palline e bastoncini. Perfino Richard Feynman, uno degli eredi intellettuali di Schrödinger, descrisse la fotosintesi in termini strettamente classici.
Ma cos’è questo mondo quantistico? Esso ci sembra molto strano, e spesso si pensa che questa stranezza sia il sintomo di una separazione fondamentale tra il mondo che vediamo attorno a noi e le sue fondamenta quantistiche. In realtà esiste un solo insieme di leggi che regola il modo in cui funziona il mondo, e sono le leggi quantistiche. Le leggi statistiche, tanto familiari, e le leggi newtoniane sono, alla fin fine, leggi quantistiche viste attraverso un filtro, che elimina tutte le cose strane (e questa è la ragione per cui ci sembrano strani i fenomeni quantistici e invece “normale” la realtà che sperimentiamo ogni giorno). Scavando più a fondo si trova la meccanica quantistica, acquattata nel cuore della realtà di tutti i giorni e che si rivela ai nostri occhi solo in determinate condizioni sperimentali, come quelle del famoso e elegante esperimento della doppia fenditura (lo trovate spiegato anche nel video in basso; nonostante l’orrendo abitino del prof. Q, è il migliore che abbia trovato in rete!). E’ un esperimento dimostrato migliaia di volte, quindi pienamente confermato, ma completamente controintuitivo e che mi stupisce ogni volta.
Per chi ha la pazienza di studiarsi questo esperimento, è evidente che il mondo quantistico, con le sue “assurde” ma verificate leggi, smette di esistere (perde la sua “coerenza”, diventando “decorente”) una volta che si effettua un’osservazione o una misura, trasformandosi in mondo classico.
Tra i due mondi, classico e quantistico, in bilico, la vita fa da ponte tra il regno classico e quello quantistico. Per esempio, gli apparati fotosintetici sono strutturati con precisione fino alla posizione delle singole particelle, e oggi il loro moto quantistico, così finemente regolato, sembra essere alla base del loro funzionamento. La cosa più strana è che le proteine o il DNA non sono macchine fatte d’acciaio e componenti rigidi; sono invece strutture flessibili e morbide, costantemente soggette alle proprie vibrazioni termiche. Una cellula è in realtà molto diversa dalle immagini, pur belle e artistiche, che spesso la raffigurano; se fosse a grandezza naturale, essa ci apparirebbe come una fabbica tumultuosa e disordinata, calda e umida, piena di operai indaffaratissimi e operosi 24h/7d. Ci si aspetterebbe che questo disordine, fatto di vibrazioni e collisioni casuali, distruggessero la delicata configurazione di atomi e molecole necessaria per mantenere il comportamento quantistico. Tutto questo trambusto cellulare, al pari dell’osservazione degli elettroni nell’esperimento della doppia fenditura, dovrebbe infatti far passare il sistema quantistico in uno stato di decoerenza. E questo infatti avviene per molti fenomeni cellulari, spiegabili convenzionalmente secondo le leggi della termodinamica classica. Eppure, esistono “sacche quantistiche” in cui fenomeni, come quelli esposti in questo articolo, seguono le leggi quantistiche senza venire perturbati dal resto. Come si riesca a mantenere la coerenza in in qusti sistemi rimane quindi un mistero.
Come funziona esattamente la fotosintesi, cioè il processo di trasformazione della materia inanimata in biomassa, ad esempio dell’aria in una mela?
Vista da lontano, una foglia è apparentemente liscia, diventa una piattaforma irregolare pavimentata di piastrelle verdi rettangolari ricoperte da blocchi rotondi più chiari, ognuno con un poro centrale. Le piastrelle verdi si chiamano «cellule epidermiche» e i blocchi rotondi si chiamano «stomi»: il loro lavoro è permettere all’aria e all’acqua (i substrati della fotosintesi) di passare attraverso la superficie della foglia e raggiungere l’interno. Una volta all’interno della foglia, si trova uno spazio ampio con cellule verdi che sembrano massi sul pavimento e spesse fibre cilindriche sul soffitto. Le fibre sono le venature della foglia, che portano acqua dalle radici (vasi xilematici) oppure trasportano gli zuccheri che si sono appena formati dalla foglia al resto della pianta (vasi floematici).
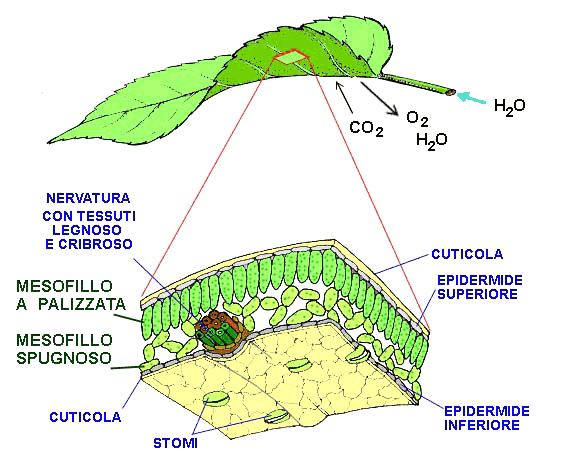
A scala cellulare, vediamo che la superficie della cellula è ricoperta di una rete di corde, un po’ come uno spesso tappeto di iuta. Questo materiale è la parete cellulare, una sorta di esoscheletro della cellula. Attraversandolo, si arriva a uno strato ceroso, la membrana cellulare, che è l’ultima barriera, impermeabile all’acqua, tra la cellula e l’ambiente esterno. Essa non è completamente liscia, ma è tempestata di piccoli fori pieni d’acqua, detti “porine”.
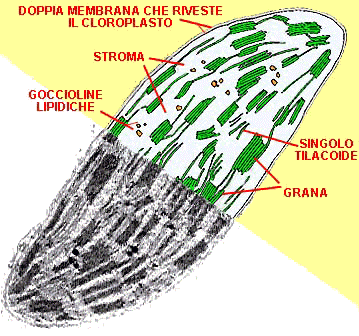
L’interno di una cellula è molto diverso dal suo ambiente esterno: è ancor più affollato e disordinato. Il citoplasma, di consistenza intermedia tra gel e liquido, è denso e vischioso. Sospesi nel gel ci sono migliaia di enzimi, responsabili dei processi metabolici della cellula: rompono i legami dei nutrienti e creano biomolecole, come carboidrati, DNA, proteine e grassi. Molti di questi enzimi sono collegati a una rete di cavi (il citoscheletro) che, un po’ come i cavi di una seggiovia, trasportano carichi da un posto all’altro della cellula. Questa rete di trasporto sembra emanare da diversi centri di smistamento, dove i cavi sono ancorati a grandi capsule verdi, che sono i cloroplasti della cellula, all’interno dei quali avviene l’azione cruciale della fotosintesi.
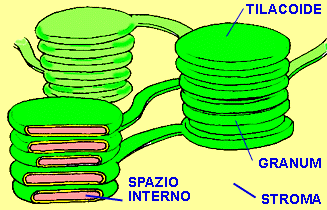
Come la cellula, il cloroplasto è anch’esso delimitato da una membrana trasparente, attraverso la quale si vedono mucchi di oggetti che sembrano monete verdi. Sono i tilacoidi, e sono pieni zeppi di molecole di clorofilla, il pigmento che rende verdi le piante. I tilacoidi sono le macchine della fotosintesi, e quando sono alimentati dai fotoni riescono a legare tra loro gli atomi di carbonio (assorbiti dall’anidride carbonica dell’aria) per costruire gli zuccheri che finiranno nella nostra mela. Qui, sebbene ci siano moltissime turbolente collisioni molecolari tutt’intorno, c’è anche un impressionante livello di ordine. La membrana di superficie del tilacoide è tempestata di scoscese isole verdi, abitate da foreste di strutture che somigliano ad alberi e terminano con piattaforme pentagonali a forma di antenna. Queste antenne sono le molecole che raccolgono la luce, chiamate cromofori, di cui la clorofilla è l’esempio più noto, e sono responsabili del primo passo della fotosintesi: la cattura dei fotoni di luce.
La clorofilla è la seconda molecola più importante sul nostro pianeta (dopo il DNA). Ha una struttura bidimensionale, fatta di anelli pentagonali costituiti principalmente da atomi di carbonio e azoto, che racchiudono un atomo centrale di magnesio con una lunga coda di atomi di carbonio, ossigeno e idrogeno. L’elettrone più esterno dell’atomo di magnesio, legato solo debolmente al resto dell’atomo, può essere sbalzato dentro la gabbia di carbonio circostante mediante l’assorbimento di un fotone di energia solare, che lascia così una lacuna nell’atomo, che resta carico positivamente. Questa lacuna elettronica si può considerare astrattamente come un buco carico positivamente. L’idea è che continuiamo a considerare l’atomo di magnesio come neutro, mentre abbiamo creato, mediante l’assorbimento del fotone, un sistema che consiste di un elettrone negativo sfuggito all’atomo e la lacuna positiva lasciata nell’atomo. Questo sistema binario si chiama «eccitone» e si può considerare come una minuscola pila con un polo positivo e uno negativo, in grado di immagazzinare energia. Alla fine della giostra, gli elettroni persi, che lasciano i buchi carichi positivamente, vengono rimpiazzati dagli elettroni dell’acqua. I sistemi di fotosintesi sono l’unico luogo del mondo naturale dove l’acqua «brucia» e cede elettroni, quindi si ossida. Abbiamo quindi un’offerta di elettroni liberi grazie all’energia fornita dagli eccitoni della clorofilla, e sono elettroni che la pianta può mandare dove serve e che saranno utili, insieme all’ATP, nella seconda fase della fotosintesi, quando la CO2 (gas) è fissata in zuccheri (solidi).
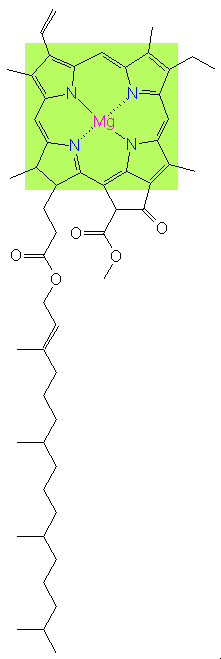
Gli eccitoni sono instabili. L’elettrone e la sua lacuna sentono una forza elettrostatica che li attrae; se si ricombinano, l’energia del fotone solare originale si disperde sotto forma di calore. Quindi, se la pianta vuole catturare l’energia solare deve trasportare l’eccitone molto rapidamente fino a un’unità di fabbrica molecolare nota come il «centro di reazione», dove avviene un processo chiamato «separazione di carica». Essenzialmente, questo significa strappare completamente un elettrone energetico dal suo atomo e trasferirlo in una molecola vicina. Questo processo crea una pila chimica più stabile di un eccitone, che si usa per alimentare le reazioni chimiche della fotosintesi. Ma i centri di reazione di solito sono abbastanza distanti, in termini molecolari (distanze di nanometri), dalle molecole di clorofilla eccitate; quindi l’energia si deve trasferire da una molecola-antenna a un’altra, nella foresta di clorofilla, per raggiungere il centro di reazione. Il trasferimento avviene grazie al fatto che la clorofilla è molto concentrata; altre molecole accanto a quella che ha assorbito il fotone possono diventare esse stesse eccitate, nei fatti ereditando l’energia dell’elettrone eccitato inizialmente, per trasferirla al proprio elettrone, nell’atomo di magnesio.
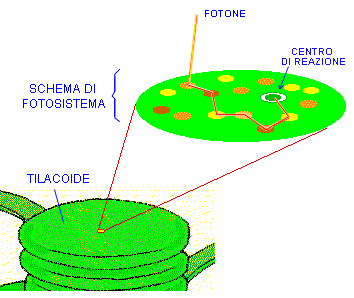
Il problema, naturalmente, è quale strada dovrebbe prendere questo trasferimento di energia. Se si avvia nella direzione sbagliata, saltando a caso da una molecola all’altra nella foresta di clorofilla, alla fine perderà la propria energia invece di consegnarla al centro di reazione. Da quale parte deve andare? Non c’è infatti molto tempo per trovare la strada prima che l’eccitazione si consumi.
Fino a poco tempo fa si pensava che questi salti di energia da una molecola di clorofilla all’altra fossero casuali, seguendo una traiettoria casuale. A volte si parla di «cammino dell’ubriaco», perché ricorda la traiettoria seguita da un ubriaco che, uscito dal bar, gira di qua e di là finché non trova finalmente la via di casa. Ma le traiettorie casuali non sono un modo efficiente per andare da qualche parte: se la casa è molto lontana, è facile che la mattina dopo l’ubriaco si trovi in un fosso dall’altra parte della città. Un oggetto che segua una traiettoria casuale tenderà ad allontanarsi dal punto di partenza di una distanza proporzionale alla radice quadrata del tempo trascorso. Se in un minuto l’ubriaco è avanzato di un metro, allora percorrerà due metri in quattro minuti, e tre metri in nove minuti. Questa descrizione non rispondeva però alla realtà, anche perché il primo passo nel processo di fotosintesi è straordinariamente efficiente. In effetti, il trasferimento dell’energia catturata dal fotone da una molecola-antenna di clorofilla al centro di reazione vanta l’efficienza più alta di tutte le reazioni naturali o artificiali conosciute: molto vicina al 100%. In condizioni ottimali, quasi tutta la quantità di energia assorbita da una molecola di clorofilla riesce ad arrivare al centro di reazione. Se il cammino seguito fosse casuale, quasi tutta l’energia perderebbe la strada. Come faccia l’energia della fotosintesi a trovare la strada fino alla sua destinazione in modo molto più efficiente degli ubriachi, o delle formiche o, se è per questo, di tutte le nostre tecnologie più efficienti, è da lungo tempo uno dei più grandi misteri della biologia.
E’ stato così che un’équipe alla University of California-Berkeley ha usato una potente tecnica spettroscopica con è riescita a sondare la struttura e la dinamica interna dei sistemi molecolari più piccoli, colpendoli con pulsazioni laser molto concentrate e brevissime. L’équipe ha impegnato la gran parte del suo tempo studiando un complesso fotosintetico chiamato «Fenna-Matthews-Olson» (FMO), presente in microbi fotosintetici (clorobi) che vivono nelle profondità di bacini ricchi di zolfo, come il Mar Nero. Per studiare il campione di clorofilla, i ricercatori hanno colpito i complessi fotosintetici con tre lampi di luce laser. Questi lampi depositano la loro energia in picchi rapidi e perfettamente sincronizzati, e generano un segnale di luce che proviene dal campione e viene rilevato da appositi apparati.
Furono messi quindi insieme i segnali che erano stati generati, della durata di 50-600 femtosecondi, per produrre un grafico dei risultati, scoprendo un segnale a spirale ascendente e discendente, che oscillava per almeno 600 femtosecondi (1 femtosecondo = 10–15 sec). Questo segnale è simile alla figura di interferenza a bande dell’esperimento della doppia fenditura (vedi filmato precedente); oppure si può considerare l’equivalente quantistico dei battimenti delle onde acustiche. Questi «battimenti quantistici» (figura in basso) mostravano che l’eccitone non prende una sola strada nel labirinto di clorofilla, ma segue piuttosto diverse vie contemporaneamente; le strade alternative agiscono un po’ come le note pulsanti di una chitarra quasi accordata: generano battimenti all’udito quando hanno circa la stessa lunghezza (permettendoci ad esempio di accordare due corde a via via adiacenti partendo da una sola – di solito il LA – accordata precisamente).
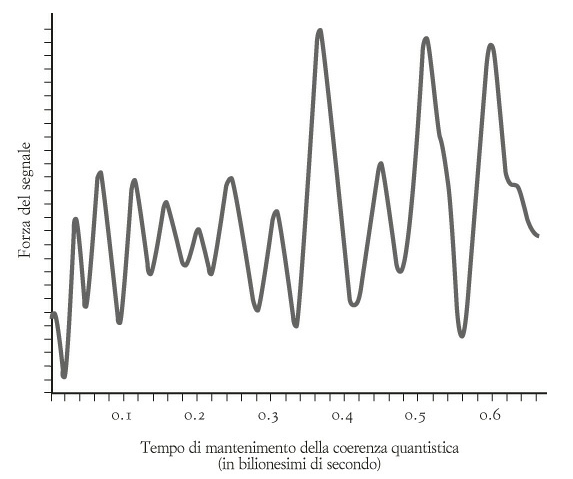
Ma, ricordiamo ancora, la coerenza quantistica è molto delicata ed estremamente difficile da mantenere in un microbo o una pianta. Il gruppo di Berkeley ipotizzava che il complesso FMO si comportasse come un computer quantistico per trovare la strada più breve verso il centro di reazione: un problema di ottimizzazione estremamente complesso. I battimenti descritti dal gruppo nel complesso FMO dimostravano effettivamente la presenza della coerenza quantistica e se ne concluse che le molecole di clorofilla mettono in pratica una nuova strategia di ricerca, chiamata «traiettoria quantistica».
Il vantaggio della traiettoria quantistica rispetto alla traiettoria casuale classica si può apprezzare tornando al nostro ubriaco che si aggira casualmente nella notte, e immaginando che nel bar da cui parte si sia rotto un tubo e l’acqua ne fluisca fuori, per la strada. Al contrario del nostro ubriacone, che deve scegliere una strada sola, le ondate d’acqua avanzano nelle strade percorrendo una distanza proporzionale al tempo trascorso, e non alla sua radice quadrata. Quindi, se in un secondo l’acqua è avanzata di un metro, in due secondi avanzerà di due metri, di tre metri in tre secondi, e così via. Ma non solo; poiché, come l’atomo in sovrapposizione nell’esperimento della doppia fenditura (che attraversa contemporaneamente le due fenditure) percorre tutte le strade possibili contemporaneamente, qualche parte dell’onda troverà sicuramente la casa dell’ubriaco molto prima di lui.
Alcuni scienziati furono molto veloci nell’osservare che gli esperimenti erano stati eseguiti con complessi FMO isolati e raffreddati a –196 °C: chiaramente una temperatura molto più fredda di qualunque temperatura compatibile con la fotosintesi delle piante, o con la vita stessa, ma bassa abbastanza da tenere a bada la fastidiosa decoerenza (la “trasformazione” dal mondo quantistico a quello classico). Quanto potevano essere rilevanti questi batteri congelati per capire quello che succede nell’interno caldo e umido delle cellule vegetali? Ben presto divenne chiaro che la coerenza quantistica non era limitata al caso del complesso FMO raffreddato. Nel 2009, furono rilevati battimenti quantistici in un altro sistema fotosintetico di batteri («fotosistema», in breve) chiamato LHC2, molto simile al fotosistema delle piante, ma questa volta a temperatura ambiente. Poi, nel 2010, si dimostrò la presenza di battimenti quantistici nel fotosistema di un gruppo di alghe criptoficee. Attorno allo stesso periodo, fu dimostrata la presenza di battimenti quantistici nello stesso complesso FMO, ma a temperatura molto più alta, questa volta compatibile con la vita. E infine, sono stati recentemente rilevati battimenti quantistici in un altro sistema LHC2, un sistema presente in tutte le piante e che contiene il 50% di tutta la clorofilla del pianeta.
La scoperta della coerenza quantistica in sistemi caldi, umidi e turbolenti come le piante e i microbi è stata quindi uno shock per i fisici quantistici, dal momento che non si comprendeva come i sistemi viventi riuscissero a proteggere e usare i loro delicati stati coerenti quantistici.



