Direttamente al succo

Le piante sono laboratori viventi di sostanze chimiche, la cui varietà oltrepassa la nostra immaginazione. Ogni anno vengono scoperti nuovi composti e potenziali medicinali sintetizzati proprio dalle piante, le quali, per la loro natura sessile, sono sottoposte a condizioni ambientali mutevoli e spesso ostili, nonché ad una vasta gamma di patogeni. Non potendosi spostare, ancorate al terreno, le piante devono ad ogni costo difendersi usando mezzi chimici. Le soluzioni che hanno funzionato, sono state setacciate dalla selezione naturale e sono arrivate fino ad oggi. Ci sono difatti molecole “antichissime”, la più famosa delle quali è la clorofilla, “inventata” nei batteri e trasmessa poi, attraverso i cloroplasti, in tutte le piante. In un articolo di qualche tempo fa, ricordavo che una parte della clorofilla è presente anche in noi come emoglobina, nei citocromi e nella vitamina B12, le cui strutture chimiche – basate sull’anello eme – sono molto somiglianti a quella della clorofilla, ma questa è un’altra storia. In parole povere, la natura conserva quello che funziona e a volte lo adatta anche a funzioni diverse (exaptation); come in una scatola di Lego, i mattoni di base sono sempre quelli ma è possibile ricombinarli a piacere. Se poi la molecola “funziona bene”, si “propaga” facilmente perché diventa un vantaggio adattativo ed evolutivo per l’organismo che la possiede ed è quindi possibile riscontrarla in piante anche non imparentate filogeneticamente.
Pensavo a tutte queste amenità, in ordine sparso come in questa introduzione, qualche settimana fa mentre stavo raccogliendo limoni in campagna. Sotto l’albero, tra spine conficcate e muri cadenti, i limoni pendevano sulla mia testa, alcuni verdi, altri giallognoli, altri ancora solo potenziali perché in fiore. L’odore prevalente era di zagara misto a quello di limone, che poi è simile a quello di quasi tutti gli agrumi (Citrus spp.), ma non solo di quelli. Lo stesso odore lo si può ritrovare in varie altre piante tra qui la citronella (Cymbopogon spp., una graminacea), dove è fortissimo, ma anche nello zenzero, nella curcuma e nel cardamomo (che appartengono alla famiglia Zingiberaceae), e io lo avverto anche in molte Lamiaceae, cioè le nostre comuni menta, lavanda, basilico, salvia, ecc., o nell’aneto e nel cumino (della famiglia Apiaeceae, parenti di carote e finocchi) o, ancora, nell’anice e nella verbena, e in alberi come il pino, il cipresso e l’eucalipto, ecc. Questi miei pensieri furono riposti in un cassetto fino a che una sera, ospite di una mia amica, mi fu rimproverato il mancato recapito come cadeau dei limoni raccolti. Tale mancanza era stata resa ancora più grave dalla passione della mia amica per le tisane, per cui mi furono mostrati una serie di agrumi e non, tutti accomunati dal tipico odore. C’era il classico limone (Citrus limon) e l’esotico lime (limetta in italiano, Citrus aurantiifolia, a buccia verde), considerati paradigmi di agrumi ma erroneamente. Difatti quasi tutti gli agrumi che conosciamo, con il loro frutto chiamato esperidio (da “Esperidi”, ninfe della mitologia greca che custodivano il giardino dei pomi d’oro di Era), sono ibridi, ad esclusione di mandarino, pomelo e cedro, che sono per così dire gli “agrumi primari”. Oltre questi due, c’erano foglie bilobate di kaffir lime (Citrus hystrix) e fusti di citronella (Cymbopogon spp.) usati in cucine orientale, e assimilabili al gusto dello zenzero, c’era anche il pepe del Sichuan (Zanthoxylum piperitum), la cui bacca ricorda quella del pepe nero, al quale non è per nulla imparentato. La storia di quest’ultima pianta è curiosa: si scartano i semi e si mangiano solo i gusci, che hanno inizialmente un sapore piccante e di limone e, dopo pochi minuti, causano un leggero intorpidimento della mucosa orale dovuto all’idrossi-alfa-sanshoolo (simile alla capsaicina dei peperoncini).

Lime, limone, pepe di Sichuan, fusto di citronella e foglia di kaffir lime.
Ho fatto tutta questa lunga dissertazione per arrivare al succo (non di limone, ma del discorso, appunto), cioè la presenza in tutte queste specie, così distanti tra loro, di una molecola chiamata limonene, oltretutto gradita al palato umano in varie culture. Il limonene è un metabolita secondario delle piante, un idrocarburo (contiene solo atomi di carbonio e idrogeno, e difatti può essere usato anche come biocarburante), ha un odore di limone/arancia o di trementina (resinoso), a seconda della sua forma enantiomerica. Il principale composto chimico presente in natura e di maggior interesse in campo industriale e merceologico è il D-limonene, ovvero l’(R)-(+)-4-isoproprenil-1-metilcicloesene. Appartiene al gruppo dei terpeni, che costituiscono le resine e gli oli essenziali di molte piante, la cui unità di base è un idrocarburo a 5 atomi di carbonio, l’isoprene. Aggiungendo varie unità di isoprene (5 atomi di carbonio alla volta, quindi), le piante sintetizzano vari composti, sia lineari (es. carotene, il mircene, il geraniolo, lo squalene, ecc.) sia ciclici (vari fitosteroli, il mentolo, il limonene, appunto, e altri ancora). Come tutti i terpeni, il limonene si scioglie meglio in alcool che in acqua, proprietà grazie alla quale possiamo godere di prodotti come il limoncello (e sue interessanti varianti, come il mandarinoncello, il Cointreau, il Grand Marnier, e altri cari compagni di serate).
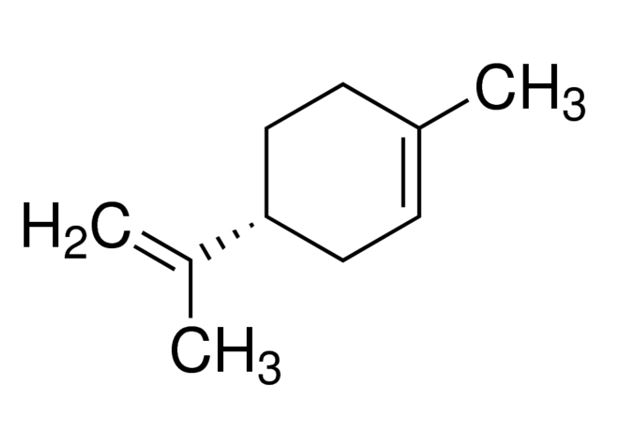 Il D-limonene
Il D-limonene
Ora, considerando che il limonene lo riscontriamo sovente e oltretutto in piante non affini, il suo vantaggio adattativo dovrebbe essere indubbio. È vero che il sapore del limonene è gradito in molte culture e si associa ad una sensazione di freschezza, ma questo non fa gli esseri umani dei vettori biologici di queste piante (anche perché ci cibiamo prevalentemente del succo e non mangiamo – e conseguentemente – defechiamo e propaghiamo semi interi). Anche l’agricoltura è relativamente recente (10.000 anni fa?) rispetto alla comparsa del limonene, per cui è difficile che l’appetibilità del composto abbia favorito addirittura la propagazione da parte degli agricoltori. Rimane quindi un vantaggio ancestrale e lontano che, a pensarci bene, abbiamo usato in passato e usiamo anche noi oggi: l’uso del limonene come insetticida e come antimicrobico (contro batteri e, in minor misura, funghi), che è poi l’uso prevalente che ne fanno piante. Noi stessi usiamo le candele alla citronella per tenere lontane le zanzare, e gli antichi egizi includevano oli essenziali di agrumi nel loro nécessaire per l’imbalsamazione dei cari estinti, al fine di arrestare l’inevitabile decomposizione microbica. E difatti, da un rapido esame di articoli scientifici sul tema (vedi lunga lista alla fine), le piante sintetizzano il limonene come difesa chimica contro molti patogeni (batteri, funghi e nematodi) e come deterrente contro gli insetti erbivori e/o che depongono uova sui/nei tessuti della pianta, uova da cui emergono voraci larve mangiafoglie.

Attività antimicrobica contro Xanthomonas oryzae da parte del (S)-limonene (riga b) e del suo enantiomero (R)-limonene (riga c). Gli aloni scuri intorno alla carta imbevuta di limonene indicano l’inibizione della crescita batterica (da Lee et al., 2016).
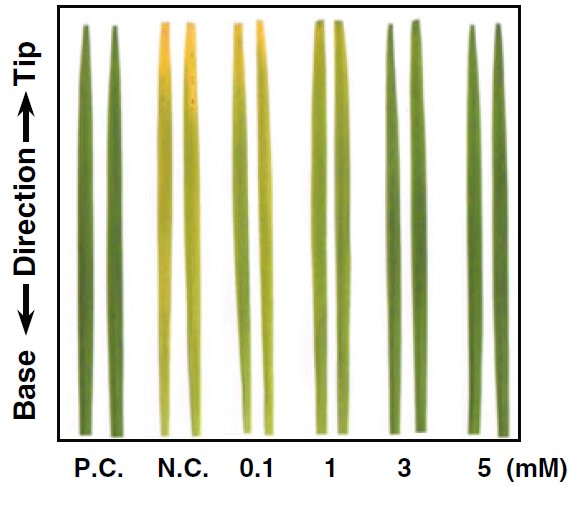
Controllo positivo (P.C.), foglie infettate (controllo negativo, N.C.) e pretrattamenti con varie concentrazioni di (S)-limonene in foglie di riso infettate da Xanthomonas oryzae (Lee et al., 2016).
Spesso il limonene è solo un prodotto intermedio, un precursore del carvone, un terpenoide dall’odore di menta o di cumino, a seconda della forma enantiomerica, che spesso ha capacità insetticida e antimicrobica anche maggiori di quelle del limonene. Il problema è che un segnale chimico non è “positivo” o “negativo” di per sé ma la risposta che induce dipende dal recettore dell’organismo bersaglio. Si potrebbe pensare quindi che elevati livelli di limonene siano favoriti nelle piante in quanto conferirebbero una maggiore protezione, ma ciò non è sempre vero. In arancio, ad esempio, livelli troppo alti di limonene fungono da deterrente anche per alcuni microorganismi utili per la pianta, i quali hanno capacità antibiotiche nei confronti di microorganismi patogeni o che favoriscono la germinazione dei semi della pianta stessa. Anche alcuni impollinatori sono attratti dal limonene, cosa che spiegherebbe perché negli agrumi i frutti, dove viene prodotto il limonene, si accompagnano spesso ai fiori. Per mantenere questo equilibrio, le piante regolano la produzione di limonene e la confinano in determinati organi e in determinati periodi. La faccenda è anche più complicata di quanto sembri perché il limonene sembra attrarre le femmine di alcune specie di coleotteri, che depongono quindi le uova sulle foglie, ma ciò è in qualche modo “tollerato” dalla pianta perché altri erbivori, più dannosi delle larve di coleottero, possono accorgersi della presenza di uova sulle foglie, evitando di mangiarle. Il limonene sarebbe quindi, ameno in questo caso, una protezione indiretta che renderebbe le femmine ovopositrici, come definiscono gli autori dell’articolo, più “choosy” (termine di forneriana e triste memoria).
La produzione industriale del limonene (attenzione, possibilmente da scarti di agrumi, dal momento che, da buon idrocarburo, si può sintetizzare anche a partire da copertoni usati) è oggi in crescita a causa del suo uso in medicina come antisettico, digestivo, aromaterapico, antinfiammatorio, antiasmatico, antiossidante, chemiopreventivo e anticancerogeno a concentrazioni di 2-2000 μM. Inoltre, a concentrazioni sotto i 10.000 μM, non ha effetti genotossici né provoca danni al DNA in cellule umane. Concentrazioni molto più alte consentirebbero invece il suo utilizzo come erbicida in agricoltura biologica perché è fitotossico e citotossico su molte erbe infestanti. A causa della loro azione insetticida, soprattutto contro le larve di lepidotteri e di coleotteri, gli oli essenziali contenenti limonene possono essere usati come biopesticidi in agricoltura biologica, anche in virtù della loro complete biodegradabilità. Un’altra proprietà fondamentale del limonene è la sua azione allelopatica, per cui le specie vegetali che lo sintetizzano e lo volatilizzano hanno vantaggi, anche a distanza, nei confronti di altre specie, inibendone la crescita o la germinazione dei semi nelle vicinanze. Una dei chemotipi più interessanti a tale riguardo è Dracocephalum kotschyi, una Lamiacea iraniana che ha altissimi livelli di limonene, con spiccate attività insetticida e allelopatica.
Oltre a questi usi, il limonene può essere usato come solvente, come biomateriale e come biocombustibile, anche se questi usi sono ancora molto limitati. Considerando la sua importanza industriale (la produzione mondiale ammonta a 60.000 t/anno), il gene della limonene sintasi, il principale enzima coinvolto nella sintesi del limonene, proveniente dal limone è stato usato per produrre piante transgeniche di Camelina sativa. Il gene, che nel limone non è costitutivo, cioè non viene sempre espresso, è stato messo sotto il controllo di un promotore (interruttore) molto forte proveniente dalla pianta modello Arabidopsis thaliana, per cui si sono ottenute piante transgeniche con alti livelli di limonene. Altre ricerche simili sono state condotte con successo su altre specie (es. tabacco) e su vari microorganismi, tra cui cianobatteri, in grado di produrre alti livelli limonene. È anche vero però che l’olio essenziale di agrumi contiene dal 70 al 98% di limonene, per cui continuano ad essere le bucce dei frutti le fonti di limonene preferite dall’industria.
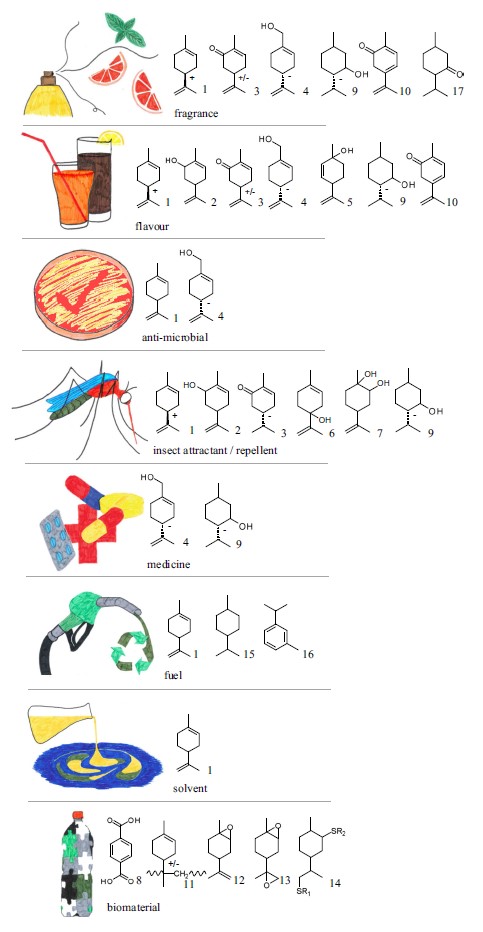
I vari usi del limonene (da Jongedijk et al., 2016).
Le piante hanno una capacità notevole di produrre e accumulare in alcuni tessuti specializzati un’ampia gamma di metaboliti e molti di essi sono escreti in forma liquida o – se hanno un basso punto di ebollizione – volatile, al punto tale che si parla di secretoma e di volatoma, cioè dell’insieme di tutte queste sostanze. I tricomi ghiandolari sono dei peletti spesso non fotosintetici sulla superficie delle foglie, sormontati da un serbatoio di olio essenziale ricoperto da un sottile strato di cuticola, che si rompe facilmente al contatto fisico. Negli esperidi degli agrumi, il limonene è accumulato in cavità secretorie nella buccia colorata (flavedo), mentre non è sintetizzato nella parte bianca (albedo). Sono questi due i tessuti dove sono presenti gli enzimi necessari (tra cui la limonene sintasi) per la produzione del limonene a partire dal glucosio e dai suoi derivati ottenuti dalla fotosintesi. La produzione è spesso concentrata in alcune fasi, di solito quando il frutto o la foglia sono a piena maturazione.
Penserete a tutte queste cose quando vi preparerete la prossima aranciata?

Tricomi ghiandolari in Cannabis spp. (fonte qui).
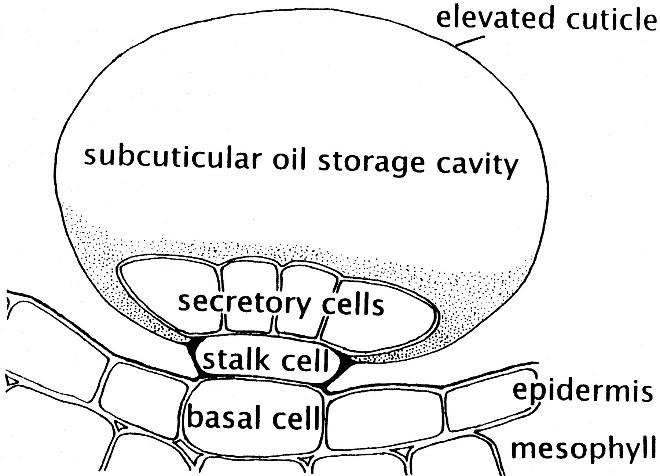
Schema di un tricoma ghiandolare.
Grazie a loro, ho scritto:
Alain Tissier (2018) Plant secretory structures: more than just reaction bags. Current Opinion in Biotechnology 2018, 49:73–79
Ali Rostaefar, Abbas Hassani, Fatemeh Sefidkon (2017) Seasonal variations of essential oil content and composition in male and female plants of Juniperus communis L. ssp. hemisphaerica growing wild in Iran. Journal of Essential Oil Research, 2017 VOL . 29, NO . 4, 357–360
Ana Rodríguez, Takehiko Shimada, Magdalena Cervera, Ana Redondo, Berta Alquezar, Marıa Jesus Rodrigo, Lorenzo Zacarıas, Lluıs Palou, Marıa M Lopez, Leandro Pena (2015) Resistance to pathogens in terpene downregulated orange fruits inversely correlates with the accumulation of D-limonene in peel oil glands. Plant Signaling & Behavior 10:6, e1028704
Avato, S. Laquale, M. P. Argentieri, A. Lamiri, V. Radicci, T. D’Addabbo (2017). Nematicidal activity of essential oils from aromatic plants of Morocco. J Pest Sci (2017) 90:711–722. DOI 10.1007/s10340-016-0805-0
Bali, Aditi Shreeya, Daizy R. Batish1, Harminder Pal Singh (2016) Allelopathic effect of aromatic plants: role of volatile essential oils. Journal of Global Biosciences, Volume 5, Number 7, 2016, pp. 4386-4395
Boni Barthélémy Yarou, Thomas Bawin, Antoine Boullis, Stéphanie Heukin, Georges Lognay, François Jean Verheggen, Frédéric Francis (2017) Oviposition deterrent activity of basil plants and their essentials oils against Tuta absoluta (Lepidoptera: Gelechiidae). Environ Sci Pollut Res. DOI 10.1007/s11356-017-9795-6
Claudinei Andrade Filomeno, Luiz Claudio Almeida Barbosa,Jose Luiz Pereira, Antonio Lelis Pinheiro, Paulo Henrique Fidencio, Ricardo Marques Montanari (2016) The Chemical Diversity of Eucalyptus spp. Essential Oils from Plants Grown in Brazil. Chem. Biodiversity 2016, 13, 1656 – 1665 DOI: 10.1002/cbdv.201600097
Diksha Sharma, HemRaj Vashist and R.B. Sharma (2015) Literature Survey on Extraction Procedure, Chemical Constituents and Pharmacological Activities of Volatile Oils and Other Extract from Citrus Plants. Singapore Journal of Scientific Research, 2015
Esmer Jongedijk, Katarina Cankar, Markus Buchhaupt, Jens Schrader, Harro Bouwmeester, Jules Beekwilder (2016) Biotechnological production of limonene in microorganisms. Appl Microbiol Biotechnol (2016) 100:2927–2938
Gun Woong Lee, Moon-Soo Chung, Mihyung Kang, Byung Yeoup Chung, Sungbeom Lee (2016) Direct suppression of a rice bacterial blight (Xanthomonas oryzae pv. oryzae) by monoterpene (S)-limonene. Protoplasma (2016) 253:683–690
Ismail Athuman, Ester Innocent, Francis Machumi, Suzana Augustino, William Kisinza (2016) Repellency properties of oils from plants traditionally used as mosquito repellents in Longido district, Tanzania. International Journal of Mosquito Research 2016; 3(1): 04-08
Ivana D. Montironi, Laura N. Cariddi, Elina B. Reinoso. Evaluation of the antimicrobial efficacy of Minthostachys verticillata essential oil and limonene against Streptococcus uberis strains isolated from bovine mastitis. Rev Argent Microbiol. 2016;48(3): 210-216
Jun-Lin Yin, Woon-Seng Wong, In-Cheol Jang, Nam-Hai Chua (2017) Co-expression of peppermint geranyl diphosphate synthase small subunit enhances monoterpene production in transgenic tobacco plants. New Phytologist (2017) 213: 1133–1144
Kamilla de Andrade Dutra, Jose Vargas de Oliveira, Daniela Maria do Amaral Ferraz Navarro, Douglas Rafael, Silva Barbosa, Jose Peroba Oliveira Santos (2016) Control of Callosobruchus maculatus (FABR.) (Coleoptera: Chrysomelidae: Bruchinae) in Vigna unguiculata (L.) WALP. with essential oils from four Citrus spp. plants. Journal of Stored Products Research 68 (2016) 25-32
M Hufnagel, AL Schilmiller, J Ali, Z Szendrei (2017) Choosy mothers pick challenging plants: maternal preference and larval performance of a specialist herbivore are not linked. Ecological Entomology (2017), 42, 33–41
Magna Galvão Peixoto, Livio Martins Costa-Júnior, Arie Fitzgerald Blank, Aldilene da Silva Lima, Thays Saynara Alves Menezes, Darlisson de Alexandria Santos, Péricles Barreto Alves, Sócrates Cabral de Holanda Cavalcanti, Leandro Bacci, Maria de Fátima Arrigoni-Blank (2015) Acaricidal activity of essential oils from Lippia alba genotypes and its major components carvone, limonene, and citral against Rhipicephalus microplus. Veterinary Parasitology 210 (2015) 118–122
Mahnaz Khanavi, Pedram Laghaei, Murray B. Isman (2017) Essential oil composition of three native Persian plants and their inhibitory effects in the cabbage looper, Trichoplusia ni. Journal of Asia-Pacific Entomology 20 (2017) 1234–1240
Merve Bacanli, A. Ahmet Basaran, Nursen Basaran (2015) The antioxidant and antigenotoxic properties of citrus phenolics limonene and naringin. Food and Chemical Toxicology 81 (2015) 160–170
Monica Borghi, De-Yu Xiei (2016) Tissue-specific production of limonene in Camelina sativa with the Arabidopsis promoters of genes BANYULS and FRUITFULL. Planta (2016) 243:549–561
Nguyen B. Qinh, Do N. Dai, Bui V. Than, Vo T Dung, Vuong T.T. Hang, Isiaka A. Ogunwande (2016) Volatile Constituents of Three Illicium Plants. Rec. Nat. Prod. 10:6 (2016) 806-811
Pasquale Cascone, Luigi Iodice, Massimo E. Maffei, Simone Bossi, Gen-ichiro Arimura, Emilio Guerrieri (2015) Tobacco overexpressing beta-ocimene induces direct and indirect responses against aphids in receiver tomato plants. Journal of Plant Physiology 173 (2015) 28–32
Po-Cheng Lin, Rajib Saha, Fuzhong Zhang, Himadri B. Pakrasi (2017) Metabolic engineering of the pentose phosphate pathway for enhanced limonene production in the cyanobacterium Synechocystis sp. PCC 6803. Scientific REPOrTS | 7: 17503 | DOI:10.1038/s41598-017-17831-y
Saroj Kumari Fagodia, Harminder Pal Singh, Daizy Rani Batisha, Ravinder Kumar Kohli (2017) Phytotoxicity and cytotoxicity of Citrus aurantiifolia essential oil and its major constituents: Limonene and citral. Industrial Crops & Products 108 (2017) 708–715
Seyed Mohammad Nabavi, Anna Marchese, Morteza Izadi, Valeria Curti, Maria Daglia, Seyed Fazel Nabavi (2015) Plants belonging to the genus Thymus as antibacterial agents: From farm to pharmacy. Food Chemistry 173 (2015) 339–347
Shahrokh Bagheri, Hassan Ahmadvand, Reza Mohammadrezaei Kkorramabadi, Peyman Khosravi (2017) Amount of limonene in different parts of plants. Geriatri Persia 2017;1(1):e03
Shatar, J. Staneva, M. Todorova, Sh. Altantsetseg (2016) The Chemical Constituents of New Essential Oils from Endemic and Sub Endemic Plants of Mongolian Gobi. Erforsch. biol .Ress. Mongolei (Halle/Saale) 2016 (13): 59-67
Siti Nur Atiqah Md Othman, Muhammad Aizam Hassan, Lutfun Nahar, Norazah Basar, Shajarahtunnur Jamil, Satyajit D. Sarker (2016) Essential Oils from the Malaysian Citrus (Rutaceae) Medicinal Plants. Medicines 2016, 3, 13; doi:10.3390/medicines3020013
Taghreed A. Ibrahima, Atef A. El-Hela, Hala M. El-Hefnawy, Areej M. Al-Taweel, Shagufta Perveen (2017) Chemical Composition and Antimicrobial Activities of Essential Oils of Some Coniferous Plants Cultivated in Egypt. Iranian Journal of Pharmaceutical Research (2017), 16 (1): 328-337
Sotero, P. Suarez, J.E. Vela, D. García de Sotero, Y. Fujii (2016) Allelochemicals of Three Amazon Plants Identified by GC-MS. International Journal of Engineering and Applied Sciences (IJEAS) ISSN: 2394-3661, Volume-3, Issue-2, February 2016
Zoya Jalaei, Mohammad Fattahi, Shahram Aramideh (2015) Allelopathic and insecticidal activities of essential oil of Dracocephalum kotschyi Boiss. from Iran: A new chemotype with highest limonene-10-al and limonene. Industrial Crops and Products 73 (2015) 109–117




