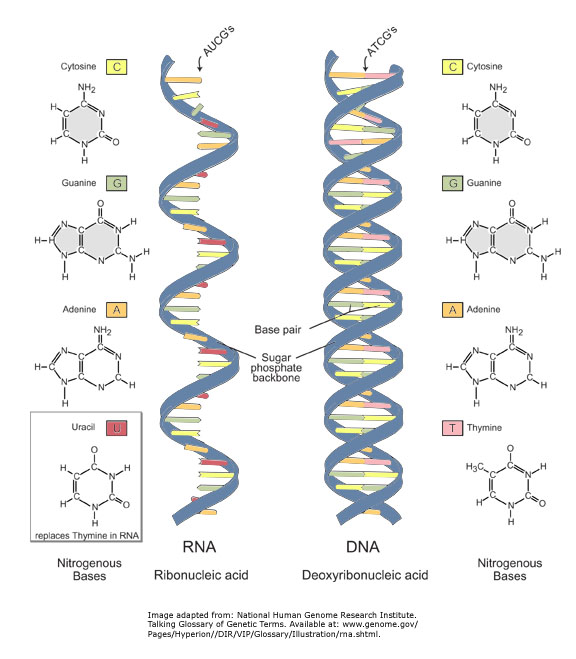
RNA family (part 1)
[segue dal post precedente]
L’altra volta abbiamo visto che gli RNA sono una grande famiglia con tre genitori (mRNA, rRNA e tRNA) e una serie di figlioletti, non meno importanti. Questi pargoli sono chiamati “RNA non codificanti”, o anche sRNA (“piccoli RNA regolatori”), perché non sono tradotti, cioè non portano informazioni per proteine. Questo fa pensare ad un originario mondo ad RNA, in cui questa molecola aveva sia un ruolo codificante che uno catalitico, quindi era in grado di portare informazioni ma anche di funzionare come un enzima, accelerando e favorendo alcune reazioni chimiche importanti per la vita. Anche se altri pensano invece che la funzione catalitica dell’RNA sia recente, il ruolo degli RNA nel controllo epigenetico degli organismi rimane di primaria importanza e per la maggior parte ancora da scoprire.
I micro RNA (miRNA) sono lunghi dalle 21 alle 26 basi e sono stati scoperti per la prima volta nel vermaccio Caenorhabditis elegans. Il precursore di questi miRNA è una molecola a doppio filamento più lunga (pre-miRNA), che viene poi tagliata in miRNA. A questi miRNA vengono aggiunti gruppi metilici per proteggerli dalla degradazione; successivamente vanno a finire nel citoplasma, dove incontrano e si legano ad un insieme di proteine (formando il complesso RISC; RNA-induced silencing complex). E’ allora che un filamento di RNA viene degradato e rimane solo la proteina con il suo frammento a singolo filamento di RNA di 21-26 basi. Questi RNA-folletto con proteina in attachment si legano agli mRNA di alcuni geni (solitamente alle porzioni non tradotte al 3’ e al 5’) impedendone la loro traduzione, oppure degradandoli. Gli mRNA sono sottoposti a questo trattamento non vengono più tradotti. Quindi niente più proteina corrispondente. Alla fine di tutto questo macello, capiamo che i miRNA intervengono nel controllo epigenetico, dal momento che non impediscono agli mRNA di essere trascritti, ma li bloccano o li degradano successivamente, in fase post-trascrizionale. Possono quindi regolare i livelli dei vari mRNA sotto il loro controllo, inducendo ad esempio una cellula di una pianta a diventare cellula radicale e un’altra in cellula del germoglio, pur avendo queste cellule lo stesso patrimonio genetico.
In questo bel video è illustrato il blocco della traduzione ad opera di un miRNA:
Gli altri folletti della famiglia degli RNA non codificanti sono i piccoli RNA nucleari (small nuclear RNA; snRNA). Queste piccole molecole, scoperte negli anni ’80, sono ricche di uracile (una delle quattro basi dell’RNA) e intervengono nel processo di splicing, in cui alcuni frammenti di mRNA (introni) sono tagliati, portando al messaggero maturo e pronto per essere tradotto in proteina. Sono inoltre coinvolti nella regolazione di alcuni fattori di trascrizione, o della stessa RNA polimerasi II o ancora nel mantenimento dei telomeri, le porzioni terminali dei cromosomi. Questi snRNA si legano a complessi proteici chiamati SNURPS (small nuclear ribonucleoproteins, snRNP), ed i più importanti sono U1, U2, U5 e U4/U6. C’è anche un interessante catalogo on-line sia di snRNA che di snRNP in Arabidopsis.
Ora che c’entra il controllo epigenetico con lo splicing? C’entra perché un mRNA appena trascritto può dare origine a diversi trascritti maturi, in base ai frammenti che vengono rimossi durante il processo di maturazione. Poiché molte proteine sono modulari, cioè formate da domini ognuno dei quali è semi-indipendente dagli altri, la presenza o l’assenza di alcuni introni nell’mRNA maturo può dare origine a diverse proteine. Questa discriminazione non è dovuta al codice genetico custodito nella “cassaforte nucleare” del DNA, ma è un controllo post-trascrizionale che può avvenire in diverse modalità in diversi organismi o in diverse popolazioni cellulari di uno stesso individuo o ancora nella stessa popolazione cellulare nelle vari fasi dello sviluppo. Siamo quindi proprio nel campo dell’epigenetica.
Nel video seguente potete vedere il processo di splicing dell’RNA:
Come vedete, la famiglia degli RNA si sta allargando, ma non siamo ancora alla fine…
Alla prossima!
[continua]
Grazie a loro, ho scritto:
Baumberger, N., Baulcombe, D.C. (2005) Arabidopsis ARGONAUTE1 is an RNA Slicer that selectively recruits microRNAs and short interfering RNAs. PNAS, 102 (33): 11928-11933
Clancy, S. (2008) RNA functions. Nature Education 1(1)
Phelps-Durr, T. L. (2010) MicroRNAs in Arabidopsis. Nature Education 3(9):51
Pontes, O., Fei Li, C., Costa Nunes, P., Haag, J., Ream, T., Vitins, A., Jacobsen, S.E., Pikaard, C.S. (2006) The Arabidopsis Chromatin-Modifying Nuclear siRNA Pathway Involves a Nucleolar RNA Processing Center. Cell 126: 79-92
Williams, R.W., Rubin, G.M. (2002) ARGONAUTE1 is required for efficient RNA interference in Drosophila embryos. PNAS, 99 (10): 6889-6894
www.plantgdb.org/SRGD/ASRG/AtsnRNA.php